메디톡스의 국내 첫 보톡스 제품 허가취소...허위 조작 등 약사법 위반으로
[우먼컨슈머= 노영조 기자] 국내 첫 ‘보톡스’ 제품으로 판매 1위인 메디톡스의 ‘메디톡신’이 허가 취소되면서 보톡스 제품에 대한 일반의 관심이 커지고 있다.
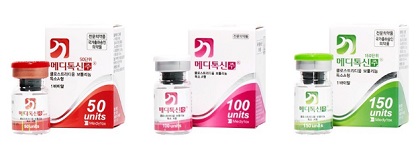
'보톡스'로도 불리는 보툴리눔 톡신 제제는 미간주름 개선 등 미용성형 시술에 사용하는 의약품이다.
국내 제약사가 개발한 보툴리눔 톡신 제품은 메디톡스의 ‘메디톡신’, 휴젤의 ‘보툴렉스’, 대웅제약의 ‘나보타’, 휴온스글로벌의 ‘리즈톡스’ 등 4종에서 메디톡신의 퇴출로 3종으로 줄었으나 메디톡신의 몫을 차지하기 위해 경쟁은 더 치열해질 전망이다.
'보톡스' 국내 시장은 1200억원 규모이며 전세계 시장은 이보다 40배나 큰 4조원에 이른다.
선두주자인 메디톡스가 생산하는 메디톡신 3품목(150·100·50단위)에 대해 식약처가 25일자로 허가취소한다고 18일 밝혔다.
이에 앞서 식약처는 메디톡신의 제조・판매・사용을 잠정 중지했다. 메디톡스가 ▲허가 내용과 다른 원액을 사용했음에도 마치 허가된 원액으로 생산한 것처럼 서류를 조작 ▲원액 및 제품의 역가시험 결과가 기준을 벗어나는 경우 적합한 것으로 허위기재 ▲조작된 자료를 식약처에 제출해 국가출하승인을 받고 해당 의약품을 시중에 판매한 혐의 때문이다.
메디톡신은 지난 2006년 메디톡스가 국내 최초로 개발한 국산 보툴리눔 톡신 제제로 인기를 각광받았던 약이다. 특히 톡신 제제는 정부가 품목허가를 내준 후에도 유통 전 제품의 품질을 한 번 더 검증(국가출하승인 제도)하는 생물제제라는 점에서 메디톡스는 더 큰 비난을 피할 수 없다.
식약처는 “이번 사건은 GMP 품질경영 원칙을 벗어난 비윤리적인 행태”라며 “제조·품질관리 자료 중 시험 과정에 대해 기록하지 않거나 시험자의 주관이 개입될 수 있는 시험(예, 동물시험)에서 이루어진 허위 기록 및 데이터 조작으로 보고 있다”고 지적했다.
다만 보툴리눔 제제에 대한 국내외 임상 논문 등을 볼 때 일정 기간 효과를 나타낸 후 체내에서 분해되므로 원액 바꿔치기 등에 따른 안전성 우려는 크지 않다고 전했다.
식약처에 따르면 메디톡스는 2012년부터 2015년까지 지속·반복적으로 원액을 바꿔치기하고 원액 및 제품의 시험성적서 등을 고의로 조작했으며, 이러한 서류 조작행위는 조직적으로 은폐되어 약사법에 따른 행정조사로는 확인에 한계가 있었으며, 검찰 수사를 통해 범죄행위가 밝혀졌다.
식약처는 서류를 조작해 부적합 제품을 유통하는 기업은 신뢰할 수 없으며, 허위조작 행위는 국민건강과 공공복리에 중대한 영향을 미칠 뿐만 아니라, 근본적으로 국내 제약산업 전반에 대한 국제 신인도에도 심각한 손상과 부정적 영향을 끼칠 수 있다고 판단했다.
한편 메디톡스 측은 “허가취소 조치는 가혹하다”며 “허가취소 집행정지 본안소송 및 가처분을 제기할 계획”이라고전했다.

